Większość komórek nowotworowych jest rozpoznawana i niszczona przez układ odpornościowy, jednak czasami dochodzi do powstania immunosupresji, przez co zmienione nowotworowo komórki stają się obojętne dla organizmu, nie są zwalczane, co może prowadzić do powstania nowotworu. Aby wzmocnić odpowiedź organizmu na obecność zmienionych komórek oraz w celu zwiększenia skuteczności ich wykrywalności zmodyfikowano komórki układu odpornościowego pacjenta. Praca opisująca procedurę wykorzystania techniki CRISPR-Cas9 w celu edycji komórek odpornościowych została opisana w prestiżowym czasopiśmie naukowym "Science".
CRISPR-Cas9 to innowacyjna technologia edycji genów, która może znaleźć zastosowanie w leczeniu wielu chorób, w tym chorób nowotworowych. Do tej pory przeprowadzono nieliczne badania z udziałem ludzi. Wstępne wyniki wydają się obiecujące.
Stadtmauer wraz z zespołem przeprowadził badanie kliniczne I fazy pacjentów z zaawansowaną chorobą nowotworową. Celem badania była ocena możliwości wykorzystania i bezpieczeństwa edycji genów metodą CRISPR-Cas9. Badanie zostało przeprowadzone na trzech pacjentach: z zaawansowanym opornym szpiczakiem (dwóch pacjentów) oraz z mięsakiem z przerzutami (jeden pacjent). Od pacjentów pobrano komórki odpornościowe – limfocyty T. Za pomocą CRISPR-Cas9 zmodyfikowano trzy geny: TRAC, TRBC i PDCD1 w celu poprawy odporności przeciwnowotworowej. Dodatkowo wprowadzono transgen NY-ESO-1, który miał wzmocnić rozpoznawalność komórek nowotworowych.
Wydajność edycji genów była podobna dla wszystkich czterech produktów, zmieniała się w zależności od pojedynczego prowadzącego RNA (sgRNA). Najwyższą skutecznością obserwowano dla genu kodującego łańcuch TCR α (TRAC), a najniższą dla genu kodującego łańcuch TCR β (TRBC). Mutacje indukowane przez CRISPR-Cas9 były wysoce specyficzne dla docelowych loci (obserwowano nieliczne zmiany niezgodne z celem). Sekwencjonowanie pojedynczych komórek wykazało, że ok. 40% miało pojedynczą mutację, 20% podwójną, 10% potrójną, a 30% pozostało niezmienionych.
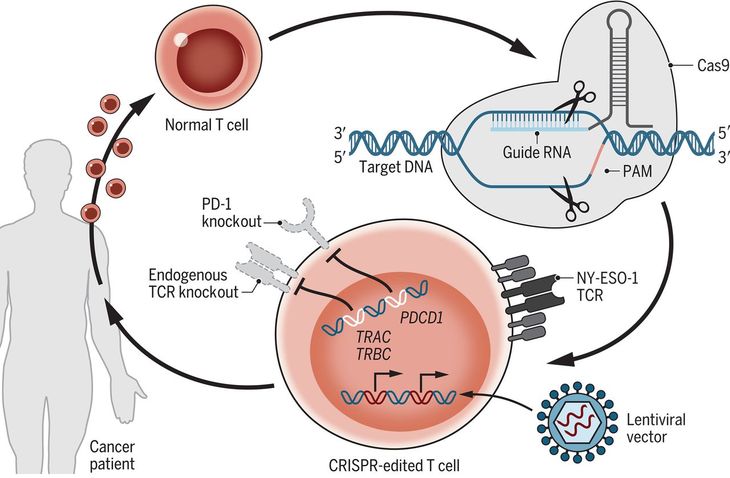
Zmodyfikowane ex vivo limfocyty T podawano we wlewie pacjentom (około 100 milionów komórek). Komórki były dobrze tolerowane przez organizm. Poziom wszczepionych komórek utrzymywał się na stałym poziomie przez cały czas trwania badania, tj. 9 miesięcy. W porównaniu do wcześniejszych prób klinicznych zaobserwowano większą skuteczność zastosowanych modyfikacji, a komórki limfocytów T wykazują większą trwałość. Korzystne było zablokowanie ekspresji endogennego TCR i PD-1 (w poprzednim badaniu endogenna ekspresja tych genów była zachowana).
Biopsje szpiku kostnego i guza wykazały obecność zmodyfikowanych komórek T w miejscu guza u wszystkich trzech pacjentów. Utrzymywanie się tych zmodyfikowanych komórek w organizmie sugeruje, że immunogenność terapii jest minimalna. Dowodzi bezpieczeństwa i skuteczności edycji genów techniką CRISPR w immunoterapii raka.
























KOMENTARZE