Fot. Obrazy z mikroskopu elektronowego przedstawiające „nanokwiaty” otrzymane z różnych białek. Zródło: dr hab. Kamila Sadowska, Instytut Biocybernetyki i Inżynierii Biomedycznej PAN
Jednym z kierunków nowoczesnej nanotechnologii jest poszukiwanie sposobów precyzyjnego dostarczania leków dokładnie w te miejsca, w których są potrzebne, z pominięciem zdrowych tkanek i ograniczeniem ogólnoustrojowej toksyczności. Takie podejście pozwala zwiększyć skuteczność terapii i jednocześnie zmniejszyć ryzyko działań niepożądanych, co jest szczególnie istotne w leczeniu nowotworów, ale też takich chorób, jak ciężkie zapalenie kości i szpiku (osteomyelitis). Osteomyelitis uznawane jest za jedną z najtrudniejszych do wyleczenia chorób zakaźnych. Rozwija się w efekcie infekcji bakteryjnej, najczęściej pałeczką ropy błękitnej lub gronkowca złocistego. Może wystąpić u każdego, choć najczęściej dotyczy dzieci poniżej 13. roku życia, pacjentów po urazach oraz osób po zabiegach chirurgicznych. W skrajnych przypadkach prowadzi do martwicy kości (co może skończyć się amputacją kończyny), a u najmłodszych – zaburzeń wzrostu i przewlekłych deformacji.
Leczenie tej choroby wymaga wielotygodniowego podawania silnych antybiotyków, takich jak cyprofloksacyna czy wankomycyna. Terapia bywa jednak trudna i nieskuteczna, ponieważ bakterie mogą znajdować się w słabo ukrwionych fragmentach kości, gdzie lek dociera w ograniczonych ilościach, lub w biofilmach, które chronią przed działaniem farmaceutyku i odpowiedzią immunologiczną organizmu. Dodatkowo tak silne środki często wywołują poważne skutki uboczne, w tym uszkodzenie nerek, wątroby czy zaburzenia hematologiczne. Z tego powodu dr hab. Kamila Sadowska, prof. Instytutu Biocybernetyki i Inżynierii Biomedycznej PAN, szukała nowych sposobów podawania antybiotyku – wprost do miejsca zakażenia, gdzie doszło do uszkodzenia kości. Badaczka wraz ze współpracownikami z Wydziału Chemii UW, Politechniki Gdańskiej i Uniwersytetu Medycznego w Lublinie wykorzystała do tego stworzone przez siebie nanostruktury. Jak opowiedziała w rozmowie z PAP dr Sadowska, mają one bardzo nietypową formę – przypominają kwiaty. – Nasze „nanokwiaty” są zbudowane z dwóch komponentów – organicznego, którym jest białko, w tym przypadku albumina surowicy bydlęcej (BSA), i nieorganicznego (zwykle fosforanów metali) – wyjaśnia.

Fot. Obrazy „nanokwiatów” Zn-BSA wykonane za pomocą skaningowego mikroskopu elektronowego przy różnych powiększeniach. Dla porównania zdjęcie kwiatów czosnku olbrzymiego (Allium giganteum). Zródło: dr hab. Kamila Sadowska, Instytut Biocybernetyki i Inżynierii Biomedycznej PAN
Taki dobór składników nie jest przypadkowy. Sama tkanka kostna ma bowiem również budowę hybrydową – składa się z części białkowej i mineralnej, co zwiększa powinowactwo nośnika do tkanki. – W badaniach wykorzystujemy albuminę surowicy bydlęcej, choć docelowo będzie to białko surowicy ludzkiej lub kolagen, które naturalnie występują w organizmach ssaków – zaznacza dr Sadowska. Ważny jest jednak także dobór składnika nieorganicznego, który decyduje o właściwościach całej struktury. Chemiczka przypomina, że chociaż pierwsze „nanokwiaty” wytwarzano z wykorzystaniem jonów miedzi, ich zastosowanie w medycynie było bardzo ograniczone, ponieważ miedź w wyższych stężeniach jest toksyczna dla organizmu. Dlatego zaczęto poszukiwać innych rozwiązań.
Jednym z kierunków badań dr Sadowskiej było wykorzystanie fosforanu wapnia w postaci hydroksyapatytu – związku, który jest naturalnym składnikiem budulcowym kości. Jego zastosowanie pozwoliło otrzymać nanostruktury przypominające budową tkankę kostną, co opisano we wcześniejszej publikacji zespołu. – Dalej jednak poszukujemy innych jonów metalu, które chętniej tworzą z białkami kompleksy „nanokwiatów”, co zwiększa wydajność reakcji, istotną dla rzeczywistych zastosowań. W najnowszej publikacji skupiliśmy się na fosforanie cynku, który spełnia te warunki – opowiada badaczka.
W celu wytworzenia „nanokwiatów” do roztworu białka w buforze fosforanowym dodaje się wodny roztwór soli wybranego metalu. Na skutek wzajemnych oddziaływań jony metalu i cząsteczki białka zaczynają się spontanicznie organizować. Formują się pierwsze niewielkie struktury, swego rodzaju zarodki krystalizacji, które stopniowo się rozrastają, tworząc charakterystyczne układy zbudowane z wielu drobnych „płatków”. Dr Sadowska zauważa, że już same „nanokwiaty”, podane w miejscu zakażenia, mogą wspomagać regenerację kości. W badaniu chodziło jednak o to, by połączyć je z cząsteczkami antybiotyku, co pozwalałoby jednocześnie aktywnie zwalczać bakterie wywołujące osteomyelitis. Kolejnym krokiem było więc wprowadzenie do materiału cyprofloksacyny.
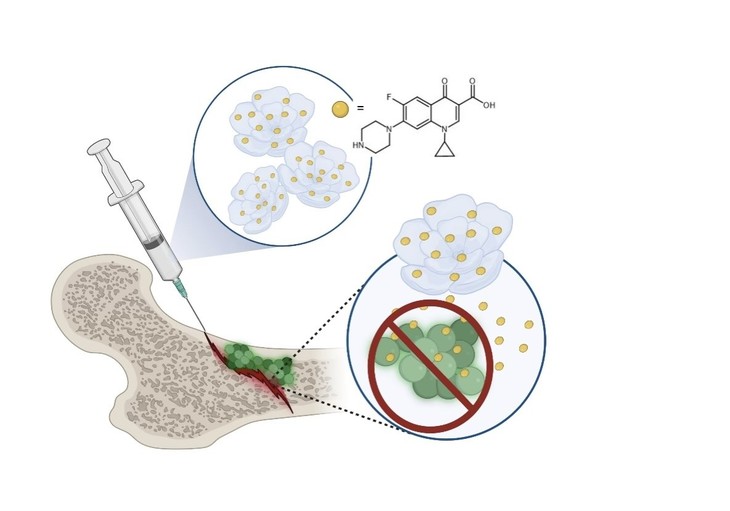
Koncepcja projektu przedstawiona graficznie. Pokazana cząsteczka to cyprofloksacyna. Źródło: dr hab. Kamila Sadowska, Instytut Biocybernetyki i Inżynierii Biomedycznej PAN
Analizy laboratoryjne potwierdziły, że cząsteczki leku skutecznie wbudowały się w strukturę nośnika, a testy biologiczne in vitro oraz na modelach zwierzęcych wykazały, że „nanokwiaty” skutecznie hamują wzrost patogennych bakterii, przy jednocześnie niskim poziomie toksyczności i dobrej tolerancji komórkowej, co wskazuje, że opracowany system może stanowić bezpieczną platformę do miejscowego dostarczania leków. – Kiedy antybiotyk podaje się ogólnoustrojowo, np. dożylnie lub doustnie, rozprowadza się on w całym organizmie, oddziałując również na zdrowe tkanki. W przypadku zapalenia kości i szpiku uzyskanie terapeutycznego stężenia leku w miejscu infekcji często wymaga wysokich dawek i długotrwałej terapii, co zwiększa ryzyko działań niepożądanych. Kość jest stosunkowo słabo ukrwiona w obszarze infekcji, co dodatkowo utrudnia leczenie. Opracowany przez nas system „nanokwiatów” umożliwia skoncentrowane dostarczenie antybiotyku bezpośrednio do miejsca zakażenia, potencjalnie zmniejszając konieczność stosowania wysokich dawek ogólnoustrojowych – podkreśla dr Sadowska.
W jej opinii takie podejście jest szczególnie istotne, ponieważ zakażenia bakteryjne w kości mogą być bardzo rozległe – czasami obejmują nawet 1/3 objętości kości i wymagają chirurgicznego usunięcia zainfekowanego szpiku, pozostawiając ubytek w tkance. Wczesne podanie antybiotyku w miejscu zakażenia pozwala skutecznie niszczyć bakterie, a wbudowana w „nanokwiaty” struktura organiczno-mineralna jednocześnie wspomaga regenerację tkanki kostnej i przyspiesza proces gojenia. Zwiększa to szansę na skuteczne leczenie i ogranicza konieczność inwazyjnych zabiegów.
Źródło: Serwis Nauka w Polsce
Autorka: Katarzyna Czechowicz (PAP)
























KOMENTARZE