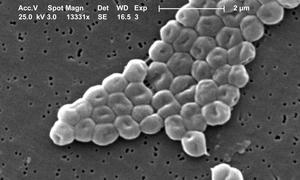
Fot. Acinetobacter baumannii, źródło: Public Health Image Library (PHIL), domena publiczna
Bakterie są ważnym elementem ludzkiego organizmu
Bakterie to mikroorganizmy, które przetrwają w najbardziej ekstremalnych środowiskach. Ludzki organizm zawiera dziesięciokrotnie więcej komórek mikroorganizmów niż własnych. Dla każdego genu człowieka przypada ok. 350 genów bakteryjnych. Naukowcy szacują, że 145 naszych genów pochodzi od bakterii, które „wtopiły się” w DNA poprzez poziomy transfer genów. Mikroflora noworodka kształtuje się w pierwszych godzinach życia i pozostaje fundamentem układu odpornościowego. Największa liczba bakterii w naszym ciele znajduje się w przewodzie pokarmowym, z największym skupiskiem w jelicie grubym.
Mikrobiom jelitowy to ekosystem pełen różnorodnych gatunków bakterii współpracujących w dynamicznej równowadze. Dominujące grupy to Firmicutes (bakterie Gram-dodatnie) i Bacteroidetes (Gram-ujemne). Osoby z nadwagą mają więcej bakterii Firmicutes, a szczupłe charakteryzuje przewaga Bacteroidetes. Bakterie w jelitach odgrywają kluczową rolę w trawieniu, rozkładają błonnik oraz produkują witaminy, np. B12, K czy biotynę. Wspierają również układ odpornościowy, zapobiegają rozwojowi infekcji. Jama ustna to potężny „teren działania” bakterii. W mililitrze śliny znajduje się aż 10 mld mikroorganizmów! Na szczęście większość z nich jest nieszkodliwa. Mikrobiom różni się w zależności od części ciała. Jest inny w jelitach, a inny w gardle lub płucach, ponieważ każde z tych środowisk ma odmienne warunki, które sprzyjają rozwojowi określonych mikroorganizmów. Mikrobiom na dłoniach, podobnie jak odciski palców, jest unikatowy dla każdej osoby i zmienia się w ciągu dnia w zależności od tego, co robimy, ale już po 24 godzinach wraca do pierwotnego stanu.
Oporność na antybiotyki
Antybiotyki to podstawowe narzędzie w walce z bakteriami. Niestety skuteczność preparatów bywa ograniczona. Bakterie wielokrotnie wystawiane na działanie leków wykształcają mechanizmy obronne. Tradycyjnie w przypadku oporności wprowadza się nowe antybiotyki, jednak ich zapasy szybko się wyczerpują. W rezultacie stajemy w obliczu realnego zagrożenia, jakim może być nowy mroczny wiek medycyny, gdy nawet drobne infekcje okażą się śmiertelne. Tradycyjnie oporność na antybiotyki kojarzona jest z trwałymi zmianami genetycznymi przekazywanymi z pokolenia na pokolenie bakterii, jednak badania pokazują, że istnieje bardziej subtelny mechanizm. Niektóre bakterie tworzą subpopulacje niereplikujących komórek, które są całkowicie odporne na działanie leków. Ten stan jest przejściowy i wynika z fenotypowych zmian, a nie genetycznych mutacji. Gdy bakterie zostaną pochłonięte przez makrofagi, mogą błyskawicznie przejść w tryb niereplikacyjny. To właśnie ten stan pozwala im unikać eliminacji przez antybiotyki. Co więcej, kiedy warunki w organizmie gospodarza poprawią się, bakterie mogą powrócić do wzrostu.
Naukowcom z Imperial College udało się zwizualizować niereplikujące komórki i odkryć sygnały prowadzące do ich formowania. W środowisku wewnątrz makrofagów Salmonella aktywuje dwa różne mechanizmy – jeden umożliwia normalną replikację, podczas gdy drugi powoduje przejście w stan niereplikacji. Warunki w makrofagach zmuszają bakterie do podjęcia decyzji – replikować czy wejść w tryb przetrwania. Zespół badaczy opracował zaawansowaną technikę wykorzystującą fluorescencyjne białka, która umożliwia śledzenie opornych komórek w zainfekowanych tkankach. W ciągu kilku minut od pochłonięcia przez makrofagi bakterie przechodzą w stan tolerancji, co czyni je niemal niezniszczalnymi dla standardowych terapii. Przy okazji w kontekście rosnącej oporności szczególną uwagę zwraca szczep Acinetobacter baumannii. Jest on jednym z najgroźniejszych patogenów szpitalnych. Ta bakteria, odporna na wiele antybiotyków, jest odpowiedzialna za liczne zakażenia, w tym zapalenie płuc, i jest wymieniana przez Światową Organizację Zdrowia jako jeden z priorytetowych problemów. Nowe badanie kliniczne, które objęło 181 pacjentów zakażonych A. baumannii, testowało dwa leki – tradycyjny lek kolistynę oraz eksperymentalny duet sulbaktam-durlobaktam. W grupie pacjentów leczonych sulbaktamem-durlobaktamem śmiertelność wyniosła 19%, natomiast w grupie leczonej kolistyną – 32%. Chociaż różnice nie są drastyczne, wskazują na to, że nowa kombinacja leków może być równie skuteczna, ale z niższym ryzykiem śmierci.
Mniejsze skutki uboczne, łatwiejsze podawanie
Ważnym atutem nowej terapii są jej łagodniejsze skutki uboczne. Kolistyna jest znana z nieprzyjemnych efektów, w tym uszkodzeń nerek. W przypadku sulbaktamu-durlobaktamu skutki uboczne były znacznie mniej nasilone. Dodatkowo podawanie sulbaktamu-durlobaktamu jest prostsze, ponieważ nie wymaga dostosowywania dawki do masy ciała pacjenta. Chociaż sulbaktam-durlobaktam nie został jeszcze zatwierdzony przez FDA, wyniki badania skłoniły komisję doradczą ds. leków przeciwdrobnoustrojowych do zalecenia jego zatwierdzenia w leczeniu zakażeń A. baumannii. Jeśli proces zatwierdzania przebiegnie szybko, nowy lek może stać się częścią standardowej opieki medycznej już w drugiej połowie roku. Choć nie jest to antybiotyk o szerokim spektrum działania, a jego skuteczność ogranicza się głównie do infekcji wywołanych przez A. baumannii, jego zastosowanie to ważny krok w walce z opornymi na leczenie bakteriami. Mimo że nie rozwiązuje to problemu globalnej oporności na antybiotyki, daje nadzieję na skuteczniejsze leczenie pacjentów w szpitalach. W połączeniu z ograniczonymi skutkami ubocznymi i prostszym sposobem podawania może to być ważny krok w stronę bezpiecznej i zarazem skutecznej terapii.























KOMENTARZE