Wirowanie analityczne odcisnęło swoje piętno w takich odkryciach, jak np. replikacja DNA, badania kompleksów rybosomalnych czy podjednostek proteasomu. W ostatnich latach metoda ta przeżywa wyraźny renesans, głównie za sprawą ciągłego doskonalenia sprzętu oraz algorytmów i programów do analizy danych.
Historia rozwoju instrumentu obejmuje kilka etapów, prawdziwych kamieni milowych. Pierwszy komercyjnie dostępny instrument Model E, opracowany w roku 1947, pomimo że znacznie mniejszy od oryginalnej wirówki Svedberga (zajmowała ona dwa piętra w budynku!), nadal przypominał ogromną szafę i był stosunkowo trudny w obsłudze, co odstraszało potencjalnych użytkowników. Prawdziwym przełomem było wprowadzenie na rynek przez firmę Beckman, odpowiednio w roku 1992 i 1996, modeli Proteomelab XL-A i XL-I. Osiągnęły one wymiar standardowej wirówki preparatywnej i wyposażone były w komputerowy układ akwizycji danych, możliwość precyzyjnej regulacji szybkości rotora oraz temperatury. Dodatkowo model XL-I pozwalał na zbieranie danych nie tylko z wykorzystaniem absorbancji, ale także interferencji. Następnym udoskonaleniem była możliwość zastosowania fluorescencyjnego systemu detekcji (modyfikacja T. Laue), co znacznie poszerzyło możliwości wirówki i zwiększyło jej selektywność i czułość. W roku 2017 Beckman-Coulter zaprezentował Optimę AUC – najbardziej zaawansowany technologicznie model wirówki. W stosunku do poprzednich instrumentów znacznie zwiększono rozdzielczość pomiaru, poprawiono stosunek sygnału do szumu, 11 x zwiększono rozdzielczość optyki interferencyjnej oraz poprzez umożliwienie jednoczesnej detekcji sygnału w 20 różnych długościach fali zwiększono precyzję pomiaru złożonych kompleksów. Wszystko to w znacznie krótszym czasie niż w przypadku poprzednich modeli.

Równolegle do rozwoju sprzętu obserwujemy doskonalenie metod analitycznych. Dostępnych jest kilka pakietów ciągle rozwijanego, bardzo zaawansowanego oprogramowania, takich jak: Sedfit/Sedphat (P. Schuck), UltraScan (B. Demeler), SedAnal (W. Stafford) czy DCDT+ (J.Philo). Oprogramowanie to jest bezpłatne, a towarzyszy mu bardzo bogata literatura oraz instrukcje obsługi, filmy instruktażowe i listy dyskusyjne.
Podstawy teoretyczne AUC
Zasady funkcjonowania wirówki analitycznej pozostają niezmienne od początku jej istnienia. Przy pomocy czułego systemu detekcji analizowany jest proces sedymentacji badanych próbek. Na cząsteczkę zanurzoną w buforze i poddaną oddziaływaniu sił grawitacyjnych działają trzy siły: siła odśrodkowa Fo, siła wyporu Fw oraz siła tarcia dynamicznego Ft. W krótkim czasie siły te równoważą się, a cząsteczka porusza się ruchem jednostajnym Fo + Fw + Ft = 0 bądź jak w przypadku równowagi sedymentacji – pozostaje nieruchoma. Upraszczając wzór, otrzymujemy definicję współczynnika sedymentacji s:
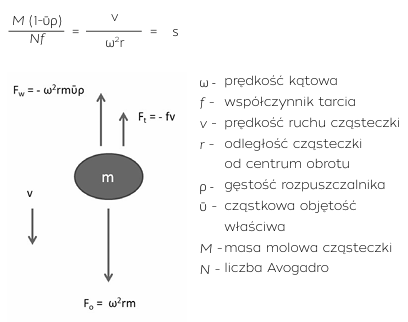
Współczynnik ten wyrażony jest w sekundach. Na cześć odkrywcy metody – Theodora Svedberga – jednostką sedymentacji jest 1 Svedberg (S) = 10–13 sekundy.
Dwa zasadnicze typy doświadczeń wirowania
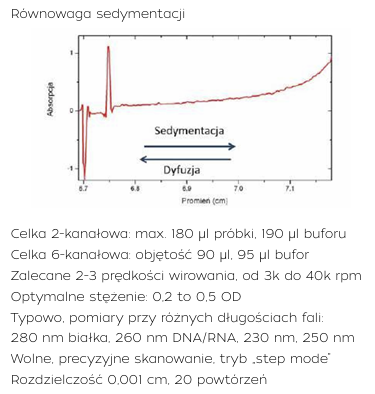
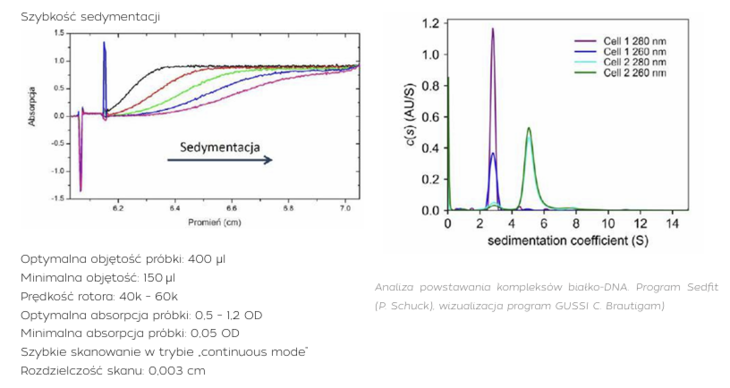
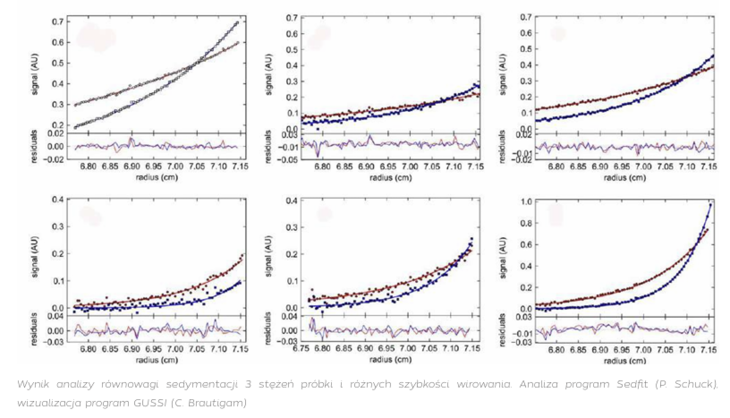
Wirówka analityczna, dzięki zainstalowanym układom optycznym, pozwala na dynamiczne śledzenie zmian rozkładu stężeń roztworu badanej próbki umieszczonej w celce pomiarowej. Doświadczenie odbywa się w ściśle kontrolowanych warunkach, w precyzyjnie wyznaczonej temperaturze oraz przy określonej szybkości kątowej rotora. Wirówka XL-I może dysponować trzema systemami detekcji: absorpcyjnym UV/VIS, interferencyjnym oraz fluorescencyjnym. Analizowana próbka umieszczona jest w rotorze tytanowym i może być wirowana z prędkościami w zakresie od 1 000 do 60 000 obrotów na minutę, co pozwala na analizę obiektów o masie od 1000 Da do 1 500 000 Da – czyli od peptydów i fragmentów kwasów nukleinowych do złożonych kompleksów makrocząsteczek czy wirusów.
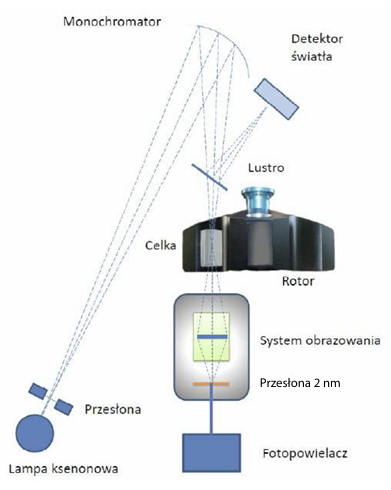
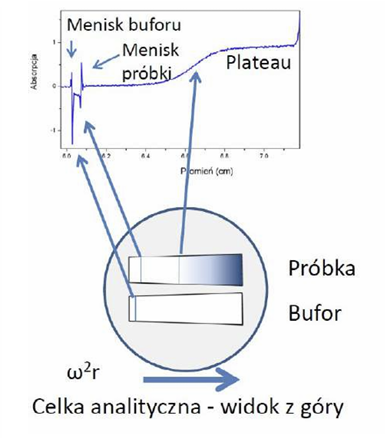
Badana próbka znajduje się w aluminiowej celce analitycznej zaopatrzonej w szafirowe lub kwarcowe okna oraz wymienny element centralny. Na wyposażeniu wirówki znajdują się m.in. następujące elementy: dwukomorowy i sześciokomorowy, zbudowane z epoksydu, dwukomorowy aluminiowy (do rozpuszczalników organicznych) oraz epoksydowy o skróconej drodze optycznej (3mm) do badania próbek w dużych stężeniach lub o dużej absorpcji.
Przewaga wirowania analitycznego nad innymi podobnymi technikami analizy biofizycznej
W ostatnim czasie pojawiło się wiele technik, które próbują konkurować z wirowaniem analitycznym. Żadna inna metoda analityczna nie jest jednak tak uniwersalna i tak udokumentowana jak AUC. Metoda ta pozwala bowiem na analizę szerokiej gamy makromolekuł w ich natywnym stanie (bez znakowania, w różnych stężeniach), w optymalnym środowisku (pH i siła jonowa buforu), bez udziału wypełnienia kolumn oddziałującego z analitem, zewnętrznych standardów czy skomplikowanej kalibracji. Może analizować takie próbki, jak: białka, peptydy, kwasy nukleinowe, przeciwciała, cząsteczki lipidowe, liposomy, pęcherzyki zewnątrzkomórkowe, micele, polimery, koloidy, nanocząsteczki, wektory wirusowe i wiele innych. Jest to także technika niedestrukcyjna, tak więc analizowane próbki mogą być następnie wykorzystane do dalszych badań lub poddane np. krystalizacji. Żadna inna technika nie dostarcza tak różnorodnych danych, uzyskanych w jednym doświadczeniu, jak np.: współczynnik sedymentacji i dyfuzji, stechiometria reakcji, stan homo- i heterooligomeryzacji, jednorodność, wzajemne oddziaływania poszczególnych komponentów, agregacja, czystość, masa, kształt, średnica czy stabilność.
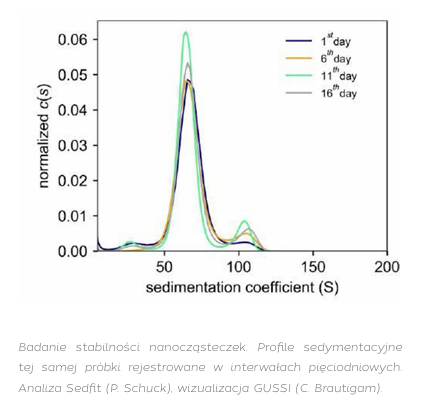
Autor: Roman Szczepanowski, PhD International Institute of Molecular and Cell Biology in Warsaw - IIMCB Biophysics and Bioanalytics Facility

























KOMENTARZE