Mechanizmy lekooporności nowotworów – od błony komórkowej po metabolizm
Lekooporność nowotworów nie jest pojedynczym zjawiskiem, lecz rezultatem nakładających się, sprzężonych mechanizmów adaptacyjnych, które pojawiają się na różnych poziomach organizacji komórki. U podstaw leży złożona plastyczność biochemiczna i biostrukturalna, dzięki której komórka nowotworowa potrafi wymknąć się cytotoksycznym bodźcom farmakoterapii. W ostatnich latach dobrze udokumentowano, że na ostateczny fenotyp MDR składają się: przebudowa błon lipidowych i „krajobrazu” białek błonowych, nadekspresja transporterów efflux (rodzina ABC), przeprogramowanie metabolizmu (glikoliza/OXPHOS, gospodarka lipidami), zmiany konformacyjne/strukturalne białek docelowych, a także komponenty „ekologii” guza – mikrośrodowisko, stan zapalny, hipoksja, a nawet udziały komórek podobnych do CSC (z ang. cancer stem cells). Z perspektywy praktycznej te wątki nie działają w izolacji – to sieć, w której zmiana jednego węzła – np. sztywności błony – przesuwa parametry transportu i aktywność pomp błonowych, a to z kolei wymusza korekty w metabolizmie oraz szlakach naprawy stresu.
Błona komórkowa to pierwsza bariera i zarazem „matryca” dla wielu procesów lekooporności. W komórkach opornych obserwuje się wzrost udziału lipidów nasyconych i cholesterolu oraz bardziej uporządkowane pakowanie łańcuchów – zjawiska te zwiększają grubość i sztywność dwuwarstwy lipidowej, modyfikują płynność i dyfuzję boczną, a w efekcie utrudniają wnikanie hydrofobowych cząsteczek leków. Na poziomie wibracyjnym manifestuje się to m.in. w regionie CH2 (ok. 2845–2880 cm-¹) i w relacjach pasm w obszarze „fingerprint”, które są czułe na stopień nasycenia, długość łańcucha i porządek fazowy. Takie przejście w kierunku stanu bardziej uporządkowanego sprzyja stabilizacji mikroobszarów raftowych, gdzie łatwiej rekrutowane są transportery efflux (np. P gp/MDR1), co wzmacnia „wypompowywanie” leku i domyka pętlę oporności. Rys. 1 wprost ilustruje tę transformację „normalna ↔ oporna błona”.
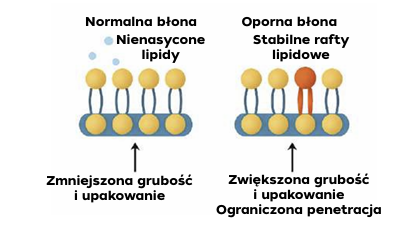
Rys. 1. Zmiany błony lipidowej w komórce opornej
W tandemie z reorganizacją lipidów zachodzi przebudowa białek błonowych oraz makromolekuł. Spektroskopowo obserwujemy to jako zmiany w Amide I (1600–1700 cm-¹) i Amide III, które odpowiadają przesunięciom równowagi α helisa/β harmonijka i mogą wskazywać na stabilizację kompleksów białkowych (w tym receptorów i pomp). Ta „rearanżacja” nie tylko zmienia farmakodynamikę (dostępność celu i sprzężenie receptorowe), lecz także wpływa na integralność cytoarchitektury, co potwierdzają liczne prace przeglądowe łączące widma Ramana z reorganizacją białek i węglowodanów w kancerogenezie i pod presją terapeutyczną.
Kolejnym filarem MDR jest nadekspresja transporterów efflux. Choć same pasma poszczególnych transporterów trudno „odizolować” w złożonej matrycy komórkowej, to pośrednie wskaźniki (sygnatury raftów lipidowych + zmiany w zestawie pasm białkowych) i metody SERS (ukierunkowane lub etykietowe) pozwalają na profilowanie fenotypu efflux, przy czym stabilne rafty dostarczają „platformy” dla ABC. Przeglądy SERS w bioanalityce i TDM konsekwentnie podkreślają wzrost możliwości wykrywania niskich stężeń markerów oporności i leków, a także rosnącą rolę uczenia maszynowego oraz AI w rozróżnianiu subtelnych różnic widmowych.
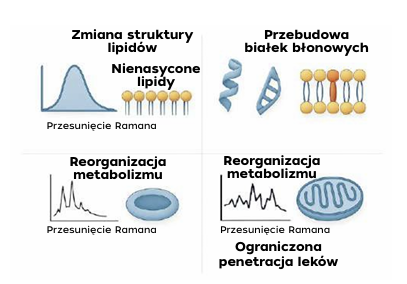
Rys. 2. Mechanizmy lekooporności widoczne w spektroskopii Ramana
Wreszcie – przeprogramowanie metaboliczne. Guzy oporne wykazują plastyczność bioenergetyczną – przełączają się między glikolizą a OXPHOS, zmieniają syntezę i utlenianie kwasów tłuszczowych oraz redystrybuują paliwa w odpowiedzi na leczenie. Zmiany te rezonują w widmach Ramana w pasmach lipidowych (1300–1740 cm-¹) kwasów nukleinowych i wybranych koenzymów, a skorelowane obrazowanie Raman + FLIM (NADH/FAD) pozwala odczytywać stan redoks i frakcje związane/wolne koenzymów jako wskaźniki aktywności metabolicznej. Z praktyki klinicznej wynika, że właśnie te adaptacje decydują o „drug tolerant persisters”, które przeczekują presję leku i odtwarzają guz.
Dlaczego potrzebujemy spektroskopii Ramana w badaniach nad lekoopornością?
Jak wspomniano powyżej, MDR obejmuje: nadekspresję transporterów efflux (ABC, np. P-gp), przebudowę błon prowadzącą do spadku przepuszczalności, przełączenia metaboliczne (glikoliza/OXPHOS), zmiany celu molekularnego i unikanie apoptozy. Jest to zjawisko wieloskładnikowe i dynamiczne, dlatego wymaga technik, które równocześnie „widzą” chemię i strukturę w żywych komórkach, najlepiej bez znaczników, które mogłyby wpływać ma metabolizm komórek. Właśnie spektroskopia Ramana dostarcza taki molekularny odcisk palca, łącząc informację jakościową i ilościową – a dzięki obrazowaniu hiperspektralnemu – także przestrzenną (mapy chemiczne). Dla badań nowotworowych kluczowe znaczenie mają sygnały pochodzące od:
* lipidów (zmiany nasycenia, długości łańcuchów, stopnia upakowania),
* białek (przegrupowania struktur α helisy i β harmonijki),
* kwasów nukleinowych (intensywność i przesunięcia pasm fosforanowych),
* metabolitów (np. NADH, mleczan),
* komponentów cytoszkieletu.
W komórkach opornych obserwuje się zwykle wzrost sygnałów odpowiadających nienasyconym lipidom, zmianę proporcji pasm Amide I/Amide III, a także większe zróżnicowanie widmowe wynikające z heterogenności metabolicznej. Te różnice są kluczem do identyfikacji fenotypów oporności.
Spektroskopia Ramana oferuje nieniszczącą, bezznacznikową metodę badania struktury chemicznej, orientacji lipidów, konformacji białek i ich dynamicznych zmian podczas leczenia. Analizując odciski palców wibracyjnych, rejestruje drobne modyfikacje w natywnych błonach lipidowych i fałdowaniu białek, gdy komórki nowotworowe oddziałują z lekami. Wykrycie tych subtelnych zmian ma kluczowe znaczenie dla zrozumienia, w jaki sposób nowotwory nabywają oporności, oraz projektowania narzędzi diagnostycznych do przewidywania i przeciwdziałania niepowodzeniom leczenia.
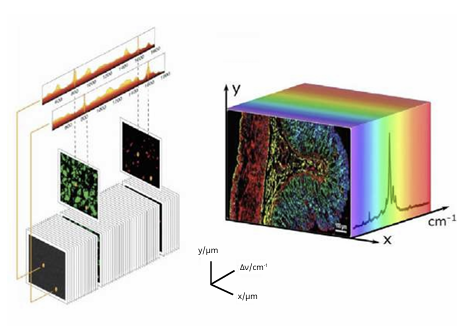
Rys. 3. Obrazowanie hyperspektralne 3D. Dane hiperkostki zawierają ogromną ilość informacji o składzie biochemicznym (w tym o białkach, lipidach, kwasach nukleinowych i węglowodanach) w każdym pikselu
W kontekście np. glejaków i innych nowotworów lekoopornych spektroskopia Ramana umożliwia:
* mapowanie składu i reorganizacji strukturalnej dwuwarstw lipidowych po ekspozycji na lek,
* monitorowanie zmian fałdowania białek związanych z mechanizmami przeżycia komórek,
* korelację integralności błony komórkowej i sygnałów molekularnych z efektami terapeutycznymi, ułatwiając wczesne wykrywanie pojawiającej się oporności.
Nowoczesne instrumenty do analizy oporności – Strada® Intelligent Raman Microscope
Inteligentny mikroskop ramanowski Strada® firmy Renishaw łączy w sobie zaawansowaną wydajność optyczną i łatwą w obsłudze automatyzację, dzięki czemu jest szczególnie odpowiedni do złożonych badań biologicznych wymagających dużej statystyki, powtarzalności wyników oraz zaawansowanych algorytmów oceny zmian widmowych próbek – tak kluczowych w badaniu lekooporności w nowotworach. Strada® Intelligent Raman Microscope oferuje zestaw funkcji, które czynią go idealnym narzędziem do badań nad lekoopornością:
* wysoką czułość i rozdzielczość (< 0,3 cm-¹) – umożliwia wykrywanie subtelnych zmian w strukturze lipidów i białek na poziomie komórkowym i subkomórkowym,
* nawigację od makro do mikro próbek – obiektyw makro i zmotoryzowana głowica obiektywu z autofocus, napędzana 8-megapikselową kamerą, pozwalają użytkownikom łatwo lokalizować i namierzać obszary zainteresowania, kolejkować pomiary, zwiększając statystykę – od obrazów całych komórek po przedziały subkomórkowe,
* szybkie obrazowanie (1400 widm/s) – pozwala na tworzenie map ramanowskich całych populacji komórek w krótkim czasie,
* LiveTrack™ i automatyczne utrzymanie ostrości – zapewnia stabilne obrazowanie nawet na nierównych powierzchniach tkankowych,
* inteligentne oprogramowanie Raman Workspace™ – automatyzuje analizę danych, umożliwia porównania między próbkami i generowanie raportów,
* przetwarzanie wsadowe oparte na szablonach i niestandardowe raporty – ułatwia standaryzowane protokoły eksperymentalne, umożliwiając efektywne porównywanie krzyżowe populacji komórek kontrolnych i poddanych leczeniu,
* zgodność z regulacjami (21 CFR Part 11) – kluczowa dla badań translacyjnych i klinicznych,
* predykcyjne utrzymanie i telemetrykę – gwarantuje ciągłość pracy w intensywnych projektach badawczych,
* uproszczone zarządzanie danymi – wspiera badania o wysokiej przepustowości, niezbędne w badaniach farmakologicznych.
Przyjrzyjmy się teraz bliżej, jak spektroskopia Ramana odsłania i monitoruje mechanizmy związane z lekoopornością, lipidomiką i metabolomiką komórek
Najsilniejszą stroną spektroskopii Ramana jest to, że łączy w jednym pomiarze trzy porządki informacji: skład chemiczny, strukturę oraz – w trybie obrazowania – przestrzeń. Dzięki temu można „przetłumaczyć” abstrakcyjne pojęcia MDR na konkretne, kwantyfikowalne wskaźniki spektralne i mapy.
W praktyce badawczej zaczynamy od portretu błony. Subtelne, ale powtarzalne różnice w regionie CH i w „fingerprint” pozwalają rozróżnić komórki wrażliwe od opornych, zanim pojawią się makroskopowe skutki w testach populacyjnych. Badania single cell Raman wykazały, że intensywności i relacje pasm korelują z klasycznymi testami cytotoksyczności (korelacje z MTT dochodzą do R² ≈ 0,95), a wprowadzenie prostego współczynnika heterogeniczności (H) ujawnia, że populacje oporne są bardziej zróżnicowane widmowo od wrażliwych – to sygnał, że w kulturze „rodzi się” subpopulacja przetrwała. W obrazowaniu hiperspektralnym różnice błonowe przekładają się na mapy porządku lipidów i regiony raftowe, które można śledzić w czasie leczenia. Przypisanie poszczególnych pasm ważnych w ocenie zmian lekooporności przedstawiono w tabeli poniżej.
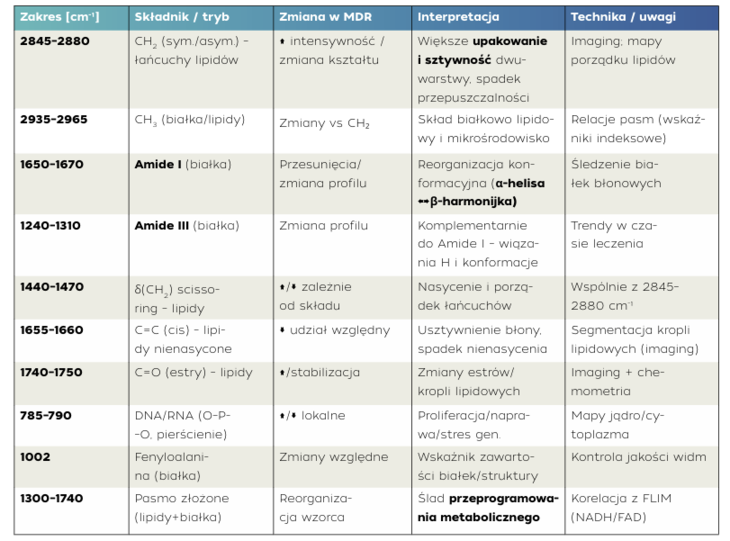
Tab. 1. Markery Ramana istotne dla oceny lekooporności (MDR)
Kiedy lek zaczyna działać, Raman pozwala rozplątywać mechanizmy kompensacyjne. Jeśli głównym celem była destabilizacja błony, a w odpowiedzi rośnie udział pasm odpowiadających lipidom nasyconym i Amide I/III zmienia się w kierunku bardziej uporządkowanych struktur białkowych, to widzimy „twardnienie” błony i stabilizację kompleksów – sygnał narastania oporności. Gdy równolegle (często w ciągu kilkunastu/kilkudziesięciu godzin) zmienia się profil lipidów kropli tłuszczowych i pojawiają się cechy przesunięcia metabolizmu (sygnatury w 1300–1740 cm-¹), interpretujemy to jako bioenergetyczne przeprogramowanie, które wspiera przetrwanie pod presją leku. Tutaj duży zysk przynosi korelacja Raman-FLIM – czasy życia NADH/FAD dopowiadają, czy system idzie ku glikolizie, czy OXPHOS, a mapy Ramana wskazują, gdzie w komórce zachodzi ten zwrot.
W obszarach wymagających szybkiej decyzji klinicznej, takich jak onkoneurochirurgia, marginesy resekcji, do gry wchodzą techniki koherentne (SRS/SRH/CARS). Dają one obraz o wysokim SNR i rozdzielczości, umożliwiając w czasie rzeczywistym wykrywanie infiltracji i różnic biochemicznych między tkanką nowotworową a prawidłową. Metaanaliza obejmująca 19 prac wykazała dla rozróżnienia „guz vs. mózg prawidłowy” czułość ~ 95,7% i specyficzność ~ 86,1%, co w praktyce przekłada się na bardziej pewne marginesy resekcji. Jeszcze dalej idą platformy AI Raman dostępne także w mikroskopie Strada® – w badaniu RAPID IDH status mutacji IDH określano śródoperacyjnie w < 3 s na próbkę, osiągając AUC ~ 0,94 i otwierając drogę do molekularnie prowadzonej resekcji. To ważne, ponieważ wiele mechanizmów oporności ma odcisk również na poziomie klasyfikacji molekularnej, a możliwość takiego rozpoznania „od ręki” zmienia decyzje terapeutyczne.
W onkologii piersi, gdzie heterogeniczność i mikrozwapnienia komplikują obraz, Raman + ML wielokrotnie osiągał ≥ 90% czułości/specyficzności w diagnostyce na materiale tkankowym i płynnej biopsji, a obrazowanie mapą chemiczną pomagało przewidywać odpowiedź na leczenie (reorganizację lipidów, ślady stresu oksydacyjnego). Te przykłady pokazują, że ten sam język widm może służyć zarówno biologii podstawowej MDR, jak i decyzjom przy łóżku pacjenta.
Wreszcie ważną niszą jest terapeutyczne monitorowanie leków (TDM) oraz detekcja biomarkerów niskich stężeń – tutaj sprawdza się metoda SERS (z ang. surface enhanced Raman spectroscopy), która dzięki wzmocnieniu pola pozwala śledzić śladowe ilości leków/metabolitów w płynach ustrojowych i – przy wsparciu algorytmów AI oraz uczenia maszynowego – rozróżniać wzorce oporności. W kontekście MDR daje to możliwość dynamicznego dostrajania dawek oraz wczesnego wykrywania niepowodzeń terapii. Spektroskopia Ramana pozwala zatem nie tylko obserwować skutki oporności, ale również odczytywać jej mechanizmy molekularne, co może mieć kluczowe znaczenie dla przyszłości medycyny precyzyjnej.
Zastosowanie spektroskopii Ramana w badaniu oporności otwiera drogę do:
* personalizowanych terapii, opartych na molekularnym profilu błon i białek,
* dynamicznego monitorowania leczenia (np. co 24–48 h),
* identyfikacji pacjentów wysokiego ryzyka nawrotu,
* opracowywania nowych leków skierowanych na membranowe mechanizmy oporności.
Technika ta, w połączeniu z AI i obrazowaniem wysokiej rozdzielczości, może stać się standardem w laboratoriach onkologicznych.
Podsumowanie
Spektroskopia Ramana dostarcza wyjątkowych możliwości śledzenia zmian molekularnych związanych z lekoopornością komórek nowotworowych. Pozwala na analizę struktur lipidowych, konformacji białek, metabolizmu oraz reorganizacji błon komórkowych w czasie rzeczywistym i bez użycia barwników. Najnowsze systemy – takie jak Strada® – sprawiają, że technika staje się szybka, automatyczna i gotowa do zastosowań translacyjnych. Raman nie tylko wyjaśnia, dlaczego komórki stają się oporne, ale także jak można temu przeciwdziałać, wspierając rozwój nowej generacji terapii przeciwnowotworowych.
Więcej informacji na temat zastosowań Ramana prod. Renishaw oraz technik połączonych, takich jak mikroskopie FLIM, AFM czy SEM, można znaleźć na stronie Renishaw. Dzięki bogatemu doświadczeniu w czołówce technologii przyrządów ramanowskich od ponad 30 lat, wspieranemu przez globalną strukturę, firma Renishaw jest partnerem, na którym można polegać teraz i w przyszłości. Zapraszamy do współpracy!
Autorka: Agnieszka Sozańska, Kierownik Sprzedaży Produktów Spektroskopowych w Renishaw
























KOMENTARZE