Fot. Laboratorium Biologii Komórki MIBMiK (2019 r.), źródło: MIBMiK
Przerzutowanie, czyli zdolność komórek nowotworowych do opuszczania guza pierwotnego i rozprzestrzeniania się na inne organy w organizmie, sprawia, że wiele chorób nowotworowych jest w dużym stopniu nieuleczalnych. Pomimo znacznego postępu w onkologii w ostatnich dziesięcioleciach, przerzutowanie jest nadal przyczyną ok. 90% zgonów pacjentów z chorobami nowotworowymi. Drugą ważną przyczyną niepowodzeń terapii onkologicznych jest utrata przez komórki nowotworowe wrażliwości na podawane leki, czyli nabycie tzw. lekooporności. Zjawisko to powoduje, że terapia przeciwnowotworowa przestaje działać, co prowadzi do wznowy choroby nowotworowej i jej progresji. AXL to receptorowa kinaza tyrozynowa, której aktywacja jest związana zarówno z przerzutowaniem, jak i lekoopornością. Jednak mimo intensywnego rozwoju inhibitorów aktywności kinazowej AXL jako leków onkologicznych, zaskakująco niewiele wiadomo na temat wewnątrzkomórkowych mechanizmów działania tego receptora.
W niedawno opublikowanym artykule w prestiżowym „Proceedings of the National Academy of Sciences of the United States of America” („PNAS”) naukowcy z Laboratorium Biologii Komórki MIBMiK opisali pierwszy interaktom (zestaw białek oddziałujących) i procesy komórkowe regulowane przez AXL, które wyjaśniają udział tego receptora w progresji nowotworowej i przerzutowaniu. Badania były prowadzone przez dr Darię Zdżalik-Bielecką w grupie prof. Marty Miączyńskiej, przy wsparciu utalentowanych naukowców na wczesnych etapach kariery naukowej: doktorantki Agaty Poświaty i magistrantki Kamili Kozik. Część badań była wykonana we współpracy z norweskimi i polskimi badaczami odpowiednio ze Szpitala Uniwersyteckiego w Oslo i Instytutu Biologii Doświadczalnej im. Nenckiego PAN.
AXL należy do podrodziny receptorów TAM (TYRO3, AXL, MER) i jest aktywowany po związaniu liganda GAS6. Nadmierna aktywacja AXL skorelowana jest z inwazyjnym fenotypem komórek nowotworowych, przerzutowaniem, lekoopornością oraz złym rokowaniem dla pacjentów. Ponadto, wiele badań sugeruje, że AXL jest zaangażowany we wnikanie do komórek wirusów, takich jak Zika czy SARS-CoV-2. Wydaje się, że AXL stanowi obiecujący cel terapeutyczny w rozwoju leczenia wspomagającego COVID-19, co dodatkowo podkreśla potrzebę lepszego scharakteryzowania procesów komórkowych regulowanych przez ten receptor. Grupa naukowców z Laboratorium Biologii Komórki, kierowanego przez prof. Martę Miączyńską, od dawna bada mechanizmy łączące endocytozę i przekazywanie sygnałów przez receptorowe kinazy tyrozynowe w warunkach fizjologicznych i patologicznych, w tym w kontekście chorób nowotworowych. W swojej najnowszej pracy naukowcy z laboratorium prof. Miączyńskiej po raz pierwszy opisali interaktom AXL, wykorzystując metodę biotynylacji zbliżeniowej BioID (ang. proximity-dependent biotin identification).
Badania wykazały, że AXL oddziałuje z wieloma białkami zaangażowanymi w regulację dynamiki cytoszkieletu aktynowego. Opisanie interaktomu receptora AXL pozwoliło odkryć, że ścieżka sygnalizacyjna GAS6-AXL aktywuje w komórce liczne procesy zależne od aktyny, takie jak: fałdowanie błony komórkowej, przebudowę miejsc adhezji i makropinocytozę. Badania naukowców z MIBMiK dowiodły, że procesy te wspólnie wzmagają inwazję komórek nowotworowych hodowanych jako trójwymiarowe sferoidy w pożywce Matrigel. W szczególności naukowcy odkryli, że aktywacja AXL indukuje dwa typy pofałdowań błon: pofałdowania obwodowe (PRs, ang. peripheral membrane ruffles) i koliste pofałdowania grzbietowe (CDRs, ang. circular dorsal ruffles). Te ostatnie były zaangażowane w przebudowę miejsc adhezji komórek do podłoża, a więc proces, który odgrywa ważną rolę podczas migracji komórek nowotworowych. Oba typy pofałdowań promowały makropinocytozę – zależną od aktyny formę endocytozy, która nie tylko pośredniczyła w internalizacji kompleksów GAS6-AXL, ale także umożliwiała wzrost komórek nowotworowych w warunkach ubogich w składniki odżywcze poprzez wzmożone pobieranie albuminy jako składnika pokarmowego. Dodatkowo naukowcy wykazali, że indukowane przez GAS6 procesy zmieniające cytoszkielet aktynowy wymagały aktywacji kinazy lipidowej PI3K i były zależne od AXL, ale nie od innego receptora TAM, TYRO3.
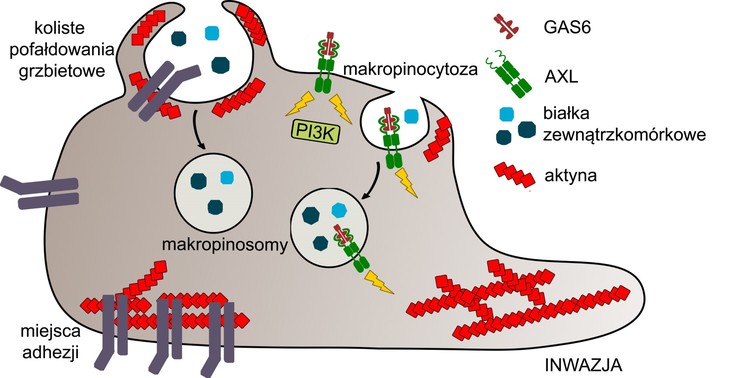
Rys. Schematyczne przedstawienie zależnych od aktyny procesów komórkowych aktywowanych przez szlak sygnałowy GAS6-AXL, które napędzają inwazję komórek nowotworowych
– Nasze badania niosą wiele istotnych implikacji. Po pierwsze, nowo zidentyfikowane białka oddziałujące z AXL stanowią cenną podstawę do dalszych badań podstawowych i translacyjnych w kierunku opracowania skutecznych terapii dla pacjentów z zaawansowaną chorobą nowotworową, w której występuje nadmierna aktywacja AXL. Po drugie, nasze badania wykazały, że GAS6 jest specyficznym ligandem dla AXL, a nie dla receptora TYRO3, co wyjaśniło długoletnie rozbieżności w literaturze naukowej dotyczącej biologii receptorów TAM. Po trzecie, odkryliśmy, że najważniejszym efektem aktywacji ścieżki sygnalizacyjnej GAS6-AXL w komórce jest rearanżacja cytoszkieletu aktynowego, co w efekcie zmienia dynamikę błon, przyleganie do podłoża, ruchliwość i metabolizm komórek. Podsumowując, nasze badania pozwoliły odkryć mechanizmy molekularne działania ścieżki GAS6-AXL jako szlaku promującego inwazję komórek nowotworowych – wyjaśnia dr Daria Zdżalik-Bielecka, inicjatorka projektu i pierwsza autorka opublikowanego artykułu.
























KOMENTARZE