Sprawdzasz wymagania renomowanego czasopisma, w którym chcesz publikować: „Prosimy podać źródło, datę i sposób otrzymania linii komórkowej, kiedy i jaką metodą linia była sprawdzana na obecność mykoplazm oraz uwierzytelniana.” Promotor niechętnie zgadza się na autentykację komórek. „Marnowanie pieniędzy, używamy tych linii od lat!” – słyszysz z korytarza, przygotowując próbki do wysyłki. Parę dni później dostajesz e-maila z wynikami i z przerażeniem odkrawasz prawdę – to zwykłe komórki HeLa! Cały doktorat podważony, reputacja laboratorium wisi na włosku, o publikacji nie ma mowy. Przerażające? W tym artykule dowiesz się, jak zapobiec temu scenariuszowi.
Wstęp
Myślisz, że błędne oznakowanie lub zanieczyszczenie linii komórkowych to rzadkość, więc nie musisz się tym martwić? Niestety, TRIP Lab świadczący usługi uwierzytelniania komórek szacuje, że aż do 36% testowanych linii jest zanieczyszczonych inną linią komórkową, mykoplazmą, wirusami lub błędnie zidentyfikowanych. Web of Science ujawniła 32 755 artykułów badawczych opartych na liniach znanych z błędnej identyfikacji. Międzynarodowy Komitet Uwierzytelniania Linii Komórkowych (The International Cell Line Authentication Committee, ICLAC) regularnie aktualizuje rosnącą listę już ponad 530 problematycznych linii, natomiast baza danych Cellosaurus zawiera ich prawie 1200 [1-5].
Te liczby są zaskakujące i z pewnością nie chcesz, aby wpłynęły na Twoją reputację. Oprócz straconego czasu i pieniędzy błędna identyfikacja komórek zagraża wiarygodnym wynikom Twojej pracy, na które czekają chorzy pacjenci. Leki, szczepionki i inne środki biomedyczne są tworzone w oparciu o wyniki badań prowadzonych na hodowlach komórkowych [6]. Błędne dane powodują duże opóźnienia w opracowywaniu terapii, a pacjenci dłużej zmagają się z objawami choroby.
Aby rozwiązać problem uwierzytelniania linii komórkowych, American Type Culture Collection (ATCC) Standards Development Organization opracowała i systematycznie doskonali standard „Authentication of Human Cell Lines: Standardization of STR Profiling” ANSI/ATCC ASN-0002-2022 STR [7]. Zgodnie z nim, ludzkie linie komórkowe mają być uwierzytelniane przy użyciu profilowania krótkich powtórzeń tandemowych (Short Tandem Repeats, STR). Stworzono też bazę danych zawierającą profile STR, elektroferogramy i inne informacje, co umożliwia identyfikację, weryfikację oraz analizę relacji między liniami komórkowymi.
STRatny wyścig z czasem? Nie z tą metodą identyfikacji!
Wiele metod, w tym analiza izoenzymów, kariotypowanie, typowanie HLA i charakteryzacja polimorfizmów długości amplifikowanych fragmentów, było stosowanych do wykrywania zanieczyszczeń krzyżowych w hodowlach komórkowych [8], jednakże najbardziej zaawansowaną i efektywną metodą jest profilowanie STR.
STR-y, krótkie, powtarzające się sekwencje DNA, charakteryzują się dużą polimorficznością między osobnikami w populacji. Można je amplifikować metodą PCR, a wielkość amplikonów wyznaczyć przez elektroforezę kapilarną, co pozwala określić liczbę powtórzeń dla danego osobnika [9]. Współczesne techniki STR wykorzystują wiele barwników, umożliwiając multipleksową analizę oraz jednoczesną elektroforezę wielu loci STR.
Ta technologia jest powszechnie stosowana na całym świecie zarówno przez ekspertów z dziedziny badań kryminalistycznych do identyfikacji osób, jak i przez naukowców do rozróżniania linii komórkowych pochodzących od różnych ludzkich dawców [10].
ICLAC zaleca uwierzytelnianie linii komórkowych na początku i końcu projektów, przy obserwacji nowych fenotypów lub podczas selekcji fenotypowej, a także przed złożeniem wniosków grantowych lub manuskryptów oraz przy zamrażaniu lub inicjowaniu nowych linii [7]. Cena usługi uwierzytelniania w stosunku do kosztów typowego projektu badawczego z użyciem linii komórkowych jest niewielka, a pomaga zabezpieczyć wyniki badań projektu badawczego.
Firma Promega, lider w dostarczaniu systemów do profilowania STR, nieustannie rozwija technologie umożliwiające skuteczną autentykację linii komórkowych według prostego schematu (rysunek 1).

Pierwszym etapem rzetelnej autentykacji linii komórkowej jest ekstrakcja DNA. Promega oferuje pełen wachlarz zestawów do izolacji kwasów nukleinowych przeznaczonych zarówno do procesów manualnych, jak i zautomatyzowanych dzięki automatom z serii Maxwell®. Zestaw Maxwell® RSC Cell DNA Purification System zapewnia szybką i efektywną izolację czystego DNA z hodowli komórkowych, przygotowując je do dalszych analiz genetycznych.
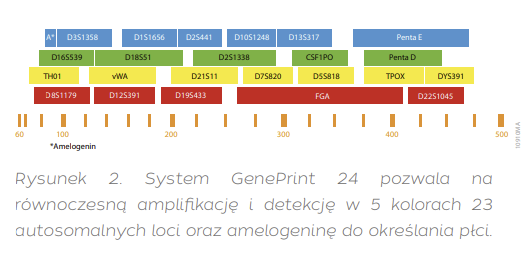
Przy użyciu odczynników z serii GenePrint®, które są „złotym standardem” uwierzytelniania w ośrodkach hodowli komórkowych, przeprowadzana jest multipleksowa reakcja PCR. Najnowszy zestaw GenePrint® 24 zawierający 24 starannie dobrane loci o wysokiej polimorficzności umożliwia uzyskanie pełnego profilu markerów STR (rysunek 2). Pozwala to na skuteczną identyfikację oraz wykrywanie zanieczyszczeń krzyżowych linii komórkowych. Ponadto system ten, dzięki wykorzystaniu różnych fluoroforów do znakowania produktów PCR, ułatwia kolejne etapy analizy.
Za pomocą elektroforezy kapilarnej amplikony są precyzyjnie rozdzielane i identyfikowane na podstawie ich rozmiaru i barwnika. Mając niewielkie, łatwe w obsłudze i uniwersalne urządzenie do elektroforezy kapilarnej Spectrum Compact CE System, możesz na bieżąco przeprowadzać genotypowanie komórek we własnym laboratorium. Alternatywnie próbki można wysyłać do wyspecjalizowanego ośrodka, który przestrzega wytycznych ANSI/ATCC.
Dane z elektroforezy są analizowane przy użyciu oprogramowania GeneMarker®HID Software, które tworzy profil genetyczny badanej linii komórkowej (rysunek 3). Każda linia komórkowa ma unikatowy wzór ilości tandemowych powtórzeń DNA, co umożliwia porównanie próbki z profilem bazowym, np. z bazy danych ATCC STR [11].

Podsumowanie
Zanieczyszczenia krzyżowe wpływają na wszystkie dziedziny biomedycyny – od artykułów badawczych opartych na liniach komórkowych, po komórki macierzyste do zastosowań klinicznych [12]. Świadomość tego problemu w społeczności badawczej rośnie, jednak błędna identyfikacja linii komórkowych nadal stanowi problem. Główne instytucje finansujące, np. Narodowe Centrum Nauki [13] i czasopisma naukowe, jak te z grupy „Nature” [14], coraz częściej wymagają, aby linie komórkowe używane w badaniach czy do produkcji farmaceutyków były testowane pod kątem tożsamości i czystości [15]. Promega dostarcza produkty, które umożliwiają potwierdzenie tożsamości komórek. Wybierając systemy, takie jak PowerPlex®, GenePrint®, Maxwell® czy Spectrum Compact CE, zyskujesz wiarygodność i rzetelność badań. Inwestując w te produkty, możesz mieć pewność, że firma Promega będzie Cię dalej wspierać w samodzielnym uwierzytelnianiu linii komórkowych – od instalacji urządzeń, po doradztwo w analizie danych.
Więcej informacji znajdziesz na stronie Promega:
Uwierzytelnianie linii komórkowych I Zautomatyzowana ekstrakcja DNA i RNA
Autorka: dr Urszula Luzarowska, Scientific Marketing Specialist w Promega GmbH

























KOMENTARZE