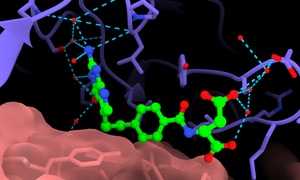
Fot. Biologia strukturalna pozwala na racjonalne, a przez to bardziej efektywne, projektowanie leków dzięki dostarczaniu dowodów o sposobie wiązania do białek, źródło: NCPS SOLARIS
Konferencja naukowa gościła wybitnych ekspertów z dziedziny biologii strukturalnej, w tym prof. Haralda Schwalbe z Uniwersytetu J.W. Goethego we Frankfurcie czy dr Lizbe Koekemoer z Centrum Odkryć Medycznych (CMD) Uniwersytetu w Oksfordzie. Obecna była także dr Isabel Moraes, biolożka strukturalna, reprezentująca Google DeepMind, jednego ze światowych liderów rozwoju sztucznej inteligencji stosowanej w nauce. – Sztuczna inteligencja będzie w coraz większym stopniu kształtować krajobraz nauk biologicznych, w tym biologii strukturalnej, za sprawą narzędzi, takich jak Project Astra – przekonywała prelegentka. Podkreśliła jednak, że przewidziane modele należy traktować jako hipotezy, które muszą być zweryfikowane eksperymentalnie. Prof. Marcin Nowotny z Międzynarodowego Instytutu Biologii Molekularnej i Komórkowej w Warszawie (IIMCB) potwierdził, że AI już dziś efektywnie wspomaga pracę biologów strukturalnych podczas prac nad określaniem atomowej budowy złożonych cząsteczek chemicznych z żywych organizmów. Wraz z nieuchronnym rozwojem technologicznym AI będzie wpływać na kolejne obszary badań, takie jak analiza danych, w tym obrazowanie w biologii czy modelowanie dużych systemów. Prof. Matthias Bochtler z IIMCB zwrócił jednak uwagę, że społeczność akademicka nie powinna bezwiednie używać gotowych narzędzi tworzonych przez firmy, lecz aktywnie uczestniczyć w ich tworzeniu.
Po co nam biologia strukturalna?
Jesteśmy zbudowani z atomów, podobnie jak cała przyroda ożywiona i nieożywiona. Atomy łączą się w cząsteczki. Wiele z cząsteczek, które funkcjonują w żywych organizmach, jest bardzo złożonych, np. DNA i RNA czy białka. Aby badać te molekuły na poziomie atomowym, potrzebne są metody, które pozwalają „powiększyć” je dziesiątki czy setki milionów razy, aby zwizualizować ich najmniejsze elementy składowe. Tu właśnie wkracza dyscyplina w naukach o życiu, zwana biologią strukturalną. Dzięki niej możemy poznać reakcje chemiczne leżące u podstaw funkcjonowania organizmów. Możemy zrozumieć, jak powstają choroby, w tym te genetyczne lub jak namnażają się wirusy. Biologia strukturalna pozwala również wizualizować, jak leki przyłączają się do cząsteczek w komórce. Dzięki temu jesteśmy w stanie optymalizować ten proces, a w konsekwencji – tworzyć nowe terapie czy poprawiać właściwości istniejących leków.
W oku synchrotronu
Nad gośćmi konferencji unosił się genius loci Narodowego Centrum Promieniowania Synchrotronowego SOLARIS Uniwersytetu Jagiellońskiego, jedynego w Polsce i pierwszego w tej części Europy ośrodka dysponującego synchrotronem. Jest to najnowocześniejsze i największe multidyscyplinarne urządzenie badawcze w kraju. Na świecie działa zaledwie kilkadziesiąt synchrotronów. Te potężne urządzenia zbudowane na planie pierścienia (krakowski SOLARIS posiada 96 m obwodu!) są akceleratorami (przyspieszaczami) elektronów i źródłem wyjątkowego światła – promieniowania synchrotronowego, które pozwala zajrzeć w głąb materii. Do synchrotronu dołączane są linie badawcze, które możemy wyobrazić sobie jako niezwykle wydajne mikroskopy. Pozwalają one dokładnie uchwycić dowolny wycinek rzeczywistości na poziomie cząsteczek i atomów. Centrum SOLARIS służy m.in. fizykom i chemikom, a obecnie na synchrotronie trwają prace nad budową nowoczesnej stacji pomiarowej do krystalografii białek, z której będą korzystać biologowie strukturalni. Znajdzie ona zastosowanie chociażby w projektach, których celem jest projektowanie nowych leków. – Zarówno biologia strukturalna, jak i technologie sztucznej inteligencji są nam niezwykle bliskie. SOLARIS inwestuje znaczne środki, w tym finansowe, w rozwój kolejnych metod badawczych, które dopełnią portfel technik istotnych dla biologii strukturalnej. Mówimy tutaj w szczególności o budowie linii badawczych dedykowanych krystalografii i rozpraszaniu promieniowania rentgenowskiego – powiedział dr hab. Jakub Szlachetko, prof. UJ, dyrektor Centrum SOLARIS. W Centrum SOLARIS obok synchrotronu funkcjonuje również laboratorium Kriomikroskopii Elektronowej SOLARIS (Cryo-EM), które powstało dzięki bezprecedensowemu solidarnemu wysiłkowi środowiska biologów molekularnych. Dysponuje ono dwoma nowoczesnymi kriomikroskopami elektronowymi. Laboratorium jest jedną z najlepszych tego typu pracowni w Europie, a przeprowadzone w nim badania stały się podstawą wielu publikacji w najlepszych międzynarodowych czasopismach naukowych.
Elektronowy przełom
Przez kilkadziesiąt lat w biologii strukturalnej dominowała metoda zwana krystalografią białek. Polega ona na uzyskiwaniu mikroskopijnych kryształów badanej substancji biologicznej, które oświetla się promieniami rentgena. W latach 90. XX w. w Poznaniu powstało pierwsze laboratorium krystalografii białek, kierowane przez prof. Mariusza Jaskólskiego. Metody te nie pozwalały jednak na poznanie struktury wielu ważnych molekuł działających w żywych organizmach, szczególnie tych bardzo złożonych i elastycznych. Około 10 lat temu nastąpił ogromny przełom w biologii strukturalnej, dzięki opracowaniu nowych metod mikroskopii elektronowej, które pozwalają wizualizować cząsteczki biologiczne z precyzją podobną do krystalografii. W 2017 r. Jacques Dubochet, Joachim Frank i Richard Henderson otrzymali Nagrodę Nobla w dziedzinie chemii za opracowanie skutecznej metody generowania trójwymiarowych obrazów cząsteczek życia. Korzystając z kriomikroskopii elektronowej, naukowcy mogą teraz zamrażać biomolekuły w ruchu i przedstawiać je z rozdzielczością atomową. Metoda ta jest jednak żmudna i długotrwała – określenie jednej struktury cząsteczki biologicznej nierzadko trwa miesiącami czy latami.
Przyszłość jest już dziś
Obecnie przeżywamy kolejny przełom. Świętym Graalem bioinformatyki (biologii komputerowej/obliczeniowej) było opracowanie metod komputerowych pozwalających na przewidywanie struktur przestrzennych cząsteczek biologicznych, bez potrzeby stosowania krystalografii czy mikroskopii elektronowej. Krok milowy w kierunku realizacji tego marzenia nastąpił mniej więcej dwa lata temu. Obecne przewidywania komputerowe budowy atomowej białek nie odbiegają już w wielu przypadkach jakością od struktur określanych metodami doświadczalnymi, a ich przygotowanie trwa sekundy, nie lata. Kolejne wyzwania to zastosowanie tych metod do przewidywania zmian kształtu cząsteczek (jest to element działania wielu z nich) czy identyfikacji nowych substancji, które mogą stać się lekami. – Dynamiczny rozwój biologii strukturalnej w ostatnich latach pozwala nam poznawać molekularne podłoże chorób. Dzięki temu możliwe jest opracowywanie terapii cechujących się wysoką skutecznością, przy minimalnych efektach ubocznych. Co więcej, stoimy teraz o krok od stosowania technik strukturalnych, np. kriotomografii elektronowej, w diagnostyce nowotworów czy chorób neurodegeneracyjnych. Nie chcemy, aby w Polsce ta szansa nas ominęła – skwitował Miłosz Ruszkowski, kierownik Zakładu Biologii Strukturalnej Eukariontów Instytutu Chemii Bioorganicznej PAN.
Szybkie zmiany, jakie zachodzą w świecie nauki, rodzą również potrzebę nowego podejścia do kształcenia przyszłych biologów. Coraz większy nacisk będzie kładziony na technologie bioinformatyczne. W laboratorium biologa strukturalnego jednym z kluczowych narzędzi będzie superkomputer z aplikacją AI, dlatego konieczny jest wzrost nakładów na infrastrukturę informatyczną, także w kontekście nauk o życiu – przekonywali uczestnicy konferencji. – Jest jasne, że ograniczenia technik opartych o AI powodują, że nie zastąpią one metod doświadczalnych w najbliższym czasie. Mogą jednak ogromnie ułatwić i przyspieszyć badania w biologii strukturalnej. Nie wiemy, czy komputery dostarczą nam lek na raka albo eliksir wiecznej młodości, jednak z pewnością nowe, coraz bardziej skuteczne narzędzia pozwolą łatwiej, szybciej i taniej prowadzić badania naukowe, a to rodzi nadzieję na rozwiązanie najbardziej palących problemów medycznych w perspektywie najbliższych dekad – podsumował prof. Marcin Nowotny. Uczestnicy konferencji iNext zgodnie stwierdzili, że pojawiające się niekiedy tezy, jakoby efekty użycia sztucznej inteligencji nie wymagały weryfikacji eksperymentalnej, stanowią zagrożenie dla nauki. Jak podkreślili dr Piotr Wilk z UJ oraz Claudia Alen Amaro z Instruct-Eric, instytucje finansujące naukę muszą mieć świadomość, że hipotezy generowane przez AI nie mogą zastąpić badań eksperymentalnych. Mogą jedynie je przyspieszyć.






















KOMENTARZE