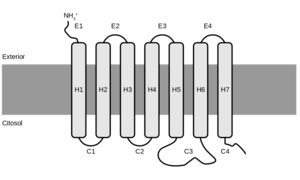
Schematyczna budowa GPCR. Widoczne siedem domen transbłonowych typu 7TM, źródło: Fred the Oysteri. Grafika wektorowa stworzona za pomocą Adobe Illustrator., CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=36317803
Celowana degradacja białek (ang. targeted protein degradation, TPD) to metoda, która przy użyciu małocząsteczkowych związków chemicznych, angażuje naturalne procesy organizmu do usuwania białek chorobotwórczych. Przewiduje się, że celowana degradacja białek zapewni nowym lekom znaczącą przewagę nad lekami klasycznymi w leczeniu chorób. Firmy Captor i Sosei Heptares początkowo skoncentrują się na identyfikacji małocząsteczkowych związków chemicznych celujących w wybrany receptor GPCR, pełniący istotną funkcję w szlaku sygnałowym związanym z chorobami układu pokarmowego. Jednym z celów współpracy jest uzyskanie informacji strukturalnych kompleksu GPCR-ligaza E3-degrader w celu ułatwienia optymalizacji kandydata na lek, a także potwierdzenia słuszności koncepcji celowanej degradacji białek w aspekcie innych receptorów GPCR oraz innych celów molekularnych. Współpraca łączy platformę projektowania leków opartego o informacje strukturalne (ang. structure-based drug design, SBDD) firmy Sosei Heptares, w tym analizę struktury celów molekularnych, oraz jej głęboką bazę wiedzy na temat farmakologii GPCR z platformą technologiczną TPD Optigradeä i szeroką wiedzą specjalistyczną na temat degradacji białek firmy Captor.
Od 2017 r. firma Captor pozyskała finansowanie w wysokości około 40 mln EUR od prywatnych inwestorów akcyjnych, jak również ze źródeł finansowania o charakterze non-dilutive (bez rozwodnienia kapitału własnego), co umożliwiło stworzenie zaawansowanej platformy TPD oraz opracowanie programów rozwoju pięciu kandydatów na leki w terapii nowotworów i chorób autoimmunologicznych. Platforma Optigradeä firmy Captor umożliwia rozwój wysoce selektywnych kandydatów na leki. Tym samym stanowi kolejną generację leków typu degrader. TPD ma na celu indukcję degradacji białek chorobotwórczych poprzez szlak degradacji zależny ligaz ubikwityny E3. Captor Therapeutics rozwija dwie klasy związków indukujących degradację, tj. kleje molekularne i degradery bifunkcyjne. Dodatkową innowacją firmy Captor jest platforma skoncentrowana na opracowanie nowych modulatorów chemicznych nowych ligaz ubikwityny E3 (ang. Ligase Ligands, Lilisä), co umożliwi w przyszłości opracowanie leków kolejnej generacji. W ramach umowy firmy będą wspólnie prowadzić program badawczy i współdzielić komercjalizację jego wyników. Firma Sosei Heptares uczestniczy w początkowych kosztach prac badawczo-rozwojowych. Szczegóły finansowe nie zostały ujawnione do wiadomości publicznej.
Miles Congreve, główny specjalista ds. naukowych firmy Sosei Heptares, skomentował – Celowana degradacja białek to obiecujący sposób podejścia do zagadnień odkrywania leków, cieszący się dużym zainteresowaniem branży farmaceutycznej, jednak dotychczas istniały pewne ograniczenia hamujące postęp w zastosowaniu tego ekscytującego podejścia do białek błonowych z rodziny GPCR. Widzimy realną możliwość poszerzenia naszej wiedzy farmakologicznej w zakresie SBDD i GPCR o obszar TPD. Receptory GPCR same w sobie odgrywają kluczową rolę w rozwoju chorób, a przy tym są często oporne na działanie leków. Z przyjemnością podejmujemy współpracę z firmą Captor, która opracowała wiele nowatorskich metod identyfikacji małocząsteczkowych związków chemicznych umożliwiających degradację białek. Cieszymy się, że możemy badać potencjał tej unikalnej kombinacji technologii, a tym samym rozwinąć nową platformę degraderów GPCR otwierającą drzwi do celów molekularnych, z którymi wiązało się jak dotąd wiele trudności.
Michal J. Walczak, dyrektor ds. naukowych firmy Captor Therapeutics, dodał – Jest to ważna współpraca zarówno dla firmy Captor, jak i dla Sosei Heptares. Jesteśmy przekonani, że skuteczne zastosowanie technologii celowanej degradacji receptorów sprzężonych z białkami G wytyczy nowe drogi w medycynie i zmaksymalizuje możliwości leczenia pacjentów. Współpraca z Sosei Heptares, światowym liderem w opracowywaniu leków celujących w receptory GPCR, to ekscytująca możliwość tworzenia nowych leków i zastosowania TPD w stosunku do rodziny białek GPCR. Z pewnością wyniki projektu będą stanowić kolejny kamień milowy potwierdzającym potencjał tej nowej technologii rozwoju leków.
























KOMENTARZE